近日,浙江大学生物系统工程与食品科学学院陈卫教授团队在国际自由基生物学领域顶级期刊《Redox Biology》(IF5 12.038)上发表研究论文“Ethyl carbamate triggers ferroptosis in liver through inhibiting GSH synthesis and suppressing Nrf2 activation”。该研究揭示了发酵食品中潜在危害物-氨基甲酸乙酯激活铁死亡途径诱发肝脏氧化损伤的作用机制。研究结果对氨基甲酸乙酯引发氧化损伤的作用机制和可能的防治措施提供了理论依据和新靶标。

氨基甲酸乙酯(Ethyl Carbamate, EC)是发酵食品在生产加工过程中产生的有害物质,国际癌症研究机构(IARC)将EC列为2A类致癌物。发酵食品如泡菜、腐乳、黄酒、白兰地等因其良好的风味深受消费者喜爱,在全球范围内销量日益增长,但EC对人类健康的风险不容忽视。现有研究表明,肝脏是EC重要的靶器官之一,其具体的毒性效应与作用机制尚不明确。因此,深入开展EC的毒性机理研究,对EC的安全防控及提高发酵食品的安全性具有重要意义。
铁死亡是一种细胞内铁依赖的新型细胞死亡形式,不同于凋亡、坏死,以脂质过氧化为特征,与部分肝脏病理状态相关。该研究团队发现EC处理会引起肝脏细胞过度氧化应激,并诱导细胞死亡;进一步研究发现EC处理导致肝脏细胞和动物肝脏铁含量和脂质过氧化水平显著升高,造成还原型GSH含量、GPX4和Ferritin蛋白表达水平下降,并引发炎症相关因子NLRP3、IL-1β和TNFα水平增加和线粒体肿胀、膜受损和嵴消失,说明EC处理激活了肝脏铁死亡过程。采用铁死亡、凋亡和坏死抑制剂处理,发现只有铁死亡抑制剂(Fer-1)能有效恢复Ferritin和GPX4蛋白表达水平,提高还原型GSH含量,并抑制了脂质过氧化和细胞毒性,表明铁死亡是EC触发肝脏毒性的主要原因;进一步研究发现EC处理显著抑制了GSH生物合成关键蛋白(GCLC和SLC7A11)表达水平,说明EC通过抑制GSH合成引发铁死亡。Nrf2是细胞抗氧化反应的主要转录因子之一,也是铁死亡的重要调控因子,Nrf2蛋白激活可通过上调SLC7A11和GCLC表达增强GSH合成。研究发现EC能降低铁死亡关键调节蛋白Nrf2活性,抑制Nrf2磷酸化修饰以及细胞核和细胞质中的表达,并减少了下游HO-1和NQO1蛋白含量,而Nrf2激动剂处理缓解了EC诱导的肝脏毒性。以上结果表明,EC通过抑制Nrf2转录活性和阻断GSH合成途径激活了肝脏铁死亡过程。
上述研究结果为发酵食品中潜在危害物氨基甲酸乙酯引发氧化损伤的作用机制和可能的防治措施提供了理论依据和新靶标,有助于构建食品安全主动防控体系,保障人民“舌尖上的安全”。
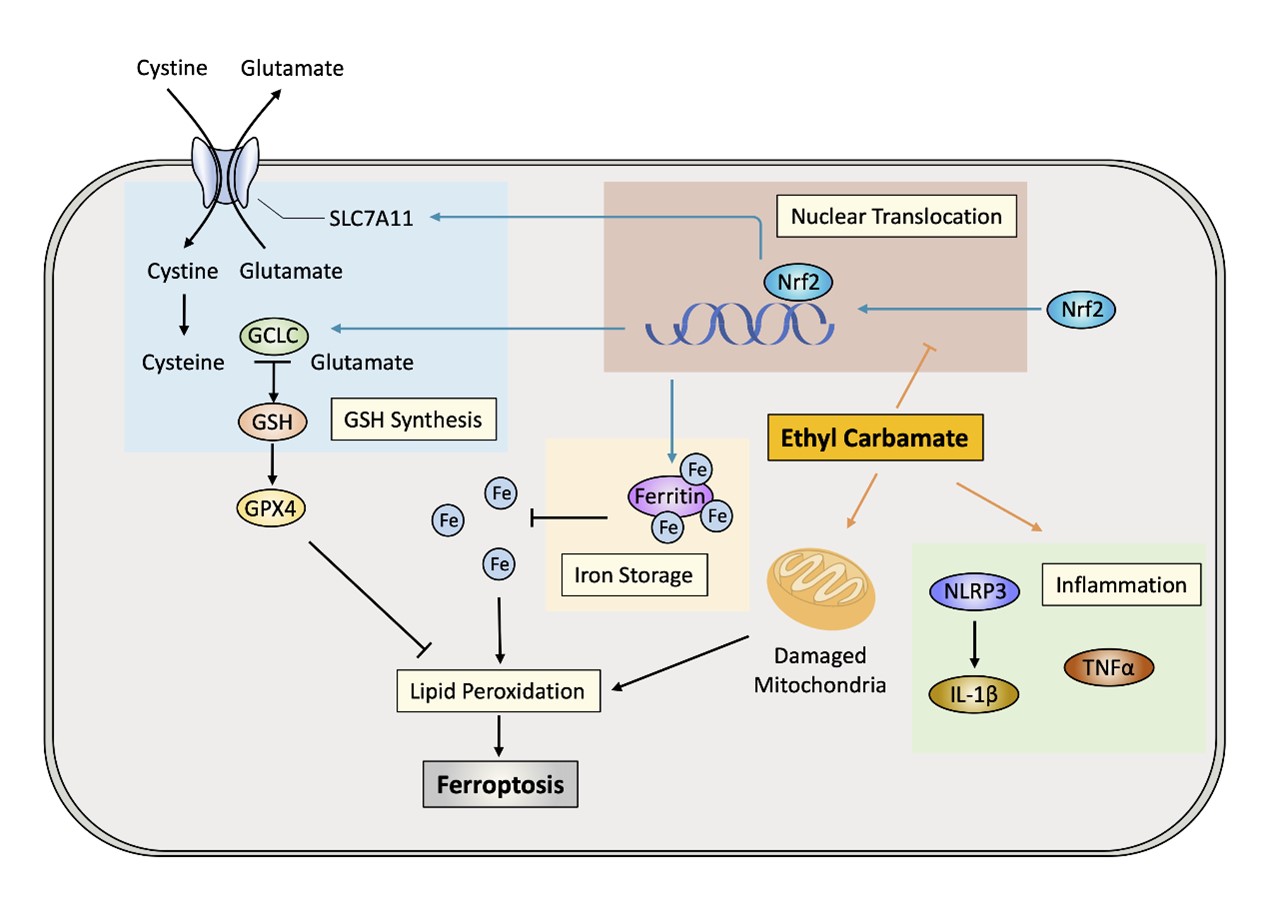
氨基甲酸乙酯激活铁死亡途径诱发肝脏氧化损伤的作用机制
陈卫教授为本文的通讯作者,博士后徐阳和博士生李玉婷为本文第一作者。本研究获得了浙江省杰出青年科学基金、国家自然科学基金和博士后创新人才支持计划等项目资助。
原文链接:https://www.sciencedirect.com/science/article/pii/S2213231722001215

